- 技术支持
电话: 4008108133
- 产品订购咨询
电话: 010-58256268
3D培养物代谢检测实践经验和核心技巧总结+案例分析
3D培养物代谢检测时间经验和核心技巧
要点总结
案例分析
精确测量表型对于理解细胞如何运作及响应其环境至关重要。这对于三维(3D)模型(如球状体和类器官)而言尤其如此,这些模型比传统单层培养物具有更高的生理相关性,同时也带来了额外的复杂性。仔细监测细胞健康与代谢对于生成既有意义又可重复的表型读数至关重要。本文重点介绍了将Promega生物发光代谢物检测法用于3D模型时的实际考量、技巧和案例研究,帮助研究人员自信地设计实验。
Promega是3D检测解决方案的领导者。无论是细胞活力、细胞毒性还是代谢物检测,我们都为您的研究需求提供强大而灵敏的工具。
Promega生物发光代谢物检测法优势
-
高灵敏度和宽动态范围:检测范围跨越飞摩尔水平至毫摩尔浓度,可捕捉小样本量中的细微变化。
-
宽检测窗口:光信号输出超过背景100倍以上,为区分真实生物学效应提供可靠依据。
-
操作流程简便:"加样-读数"操作模式最大限度减少操作步骤,降低变异度,并可无缝对接标准微孔板读数仪(图2)。
检测原理:Promega的生物发光代谢物检测法为监测关键代谢通路(包括葡萄糖利用、脂质代谢、氨基酸转运和线粒体功能)提供灵敏可靠的工具。这些检测法基于一个简单原理:代谢物特异性脱氢酶生成NAD(P)H,进而驱动前体萤光素底物转化为萤光素。在萤光素酶存在下,会产生与样品中代谢物含量成正比的光信号(图1)。
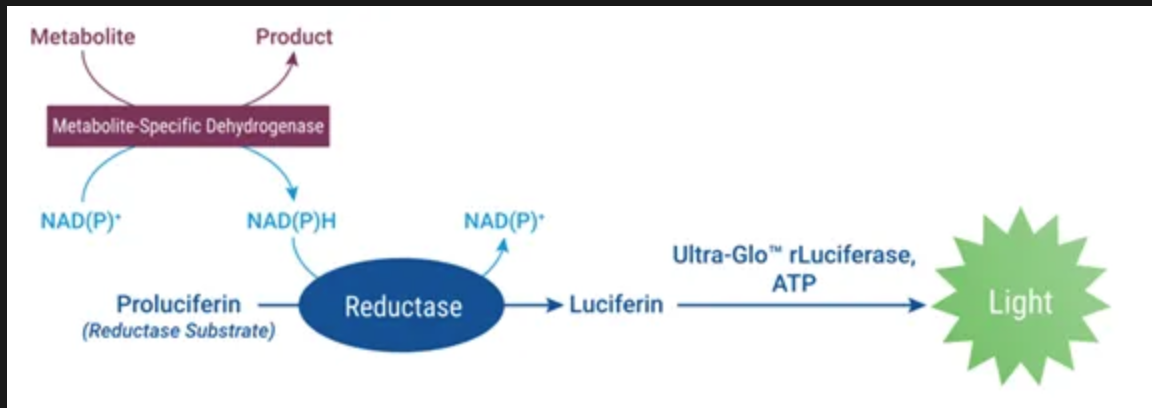
图1. Promega生物发光法代谢物检测原理。
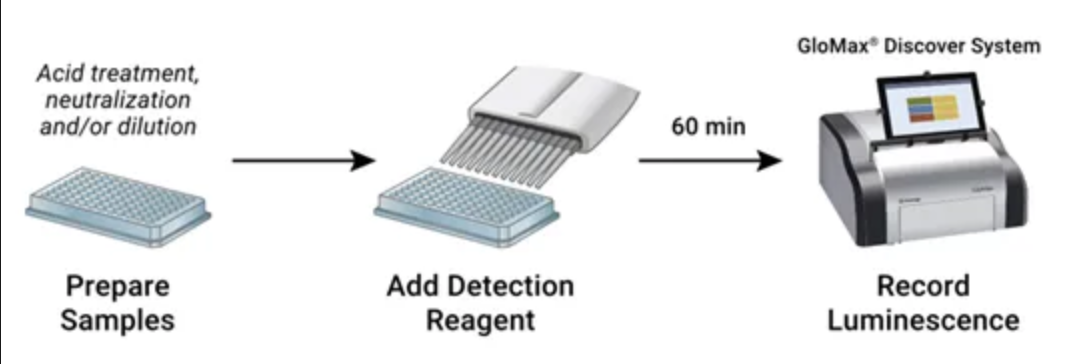
图2. 使用Promega检测法进行代谢物检测的简要工作流程。
如何为3D模型代谢物检测选择合适培养基?
培养基是代谢研究中的核心实验变量。除了支持细胞生长外,培养基定义了细胞所处的代谢物环境,因此强烈影响细胞行为及检测读数。这种影响在3D系统中被放大,因为球状体或类器官内部会形成氧气和营养物质的梯度,使得培养基配方尤为关键。MISpheroID联盟强调需要仔细报告培养基条件,以保证3D培养研究的透明度和可重复性(Nature Methods, 2021)。要了解更多关于MISpheroID知识库的目的,请阅读以下blog文章。
要点一:营养物质浓度很重要
市面上销售的培养基在关键代谢物(如葡萄糖、谷氨酰胺和丙酮酸)的浓度上差异很大。例如,葡萄糖水平可能从生理相关的5mM到超生理的25mM不等,这会显著改变细胞的代谢行为。
要点二:血清选择影响灵敏度
血清的选择增加了另一层复杂性:标准胎牛血清含有毫摩尔水平的小代谢物(如乳酸和谷氨酸),这可能会掩盖细胞水平的细微变化。透析血清可减少这些背景代谢物,并改善对消耗或分泌事件的检测。在可行的情况下,补充了特定代谢物和透析血清的确定成分基础培养基可提供最受控的条件。
要点三:保持在检测的线性范围内
同样重要的是了解您培养基中的基线代谢物浓度。Promega代谢物检测法在50–200µM范围内提供准确定量,而许多常见培养基配方中的代谢物以毫摩尔水平存在。若不进行适当稀释,样品将超出线性检测窗口,并掩盖真实的生物学变化。调整稀释因子可确保准确定量并在实验间进行有意义的比较。
要点总结:为后续代谢物检测选择培养基的最佳实践经验
-
尽可能选择生理相关的基线浓度(例如5mM葡萄糖)。
-
使用透析血清以尽量减少背景代谢物干扰。
-
记录并报告确切的培养基配方以保证可重复性。
-
稀释培养上清液使代谢物浓度进入检测法的线性范围。
3D球状体操作的实用技巧
Promega的"加样-读数"操作模式生物发光代谢物检测法非常适用于自动化和高通量工作流程。然而,球状体独特的操作挑战需要一些调整,以确保结果可重复并能扩展到高通量工作流程。
要点一:3D细胞模型对培养基移除更换敏感
更换含有单个球状体的孔中的培养基在技术上是困难的。在96孔超低吸附板中,尝试完全移除培养基经常会干扰甚至移除球状体,导致孔间差异。这对于抑制剂或化合物筛选尤其成问题,因为复孔间的一致性至关重要。
要点二:部分培养基更换在数据质量与球状体完整性之间取得平衡
为解决球状体操作挑战,我们建议采用部分更换方法,仅移除50%的培养基,并用含有抑制剂或化合物的新鲜培养基替换。该策略降低了球状体被干扰的风险,并最大限度地减少了孔间差异,使工作流程更易于自动化。部分培养基更换的一个局限性是,在处理时起始代谢物浓度仍然较高,降低了检测后续变化的灵敏度。尽管灵敏度有所降低,部分更换方法在数据质量和球状体完整性之间提供了实际的平衡,尤其在筛选背景下。
要点总结:3D球状体检测中培养基更换的最佳实践经验
-
不要完全移除培养基,仅更换约50%的体积以保持球状体完整性,同时仍提供新鲜营养物或药物暴露。
-
部分更换会导致基线代谢物水平较高,这可能降低检测微小变化的灵敏度。
-
仅含培养基的对照和零时对照对于区分处理效应与基线代谢物积累至关重要。
案例研究1:监测3D模型中的代谢物消耗和分泌
为说明培养基成分和细胞密度如何影响检测结果,我们比较了在两种培养基条件下培养的HCT116球状体的葡萄糖消耗和乳酸分泌情况:
M1:含5mM葡萄糖和5%透析血清的DMEM
M2:含25mM葡萄糖和10%胎牛血清的DMEM
将HCT116细胞以不同的起始密度(每孔1,000、2,500或5,000个细胞)铺板在超低吸附板中以形成球状体。72小时后,从每个孔收集培养上清液,并使用Glucose-Glo™ Assay和Lactate-Glo™ Assay进行分析。由于M2培养基中的基线葡萄糖浓度显著高于M1,样品用PBS稀释800倍(M2)或160倍(M1),使代谢物水平进入检测法的线性检测范围。
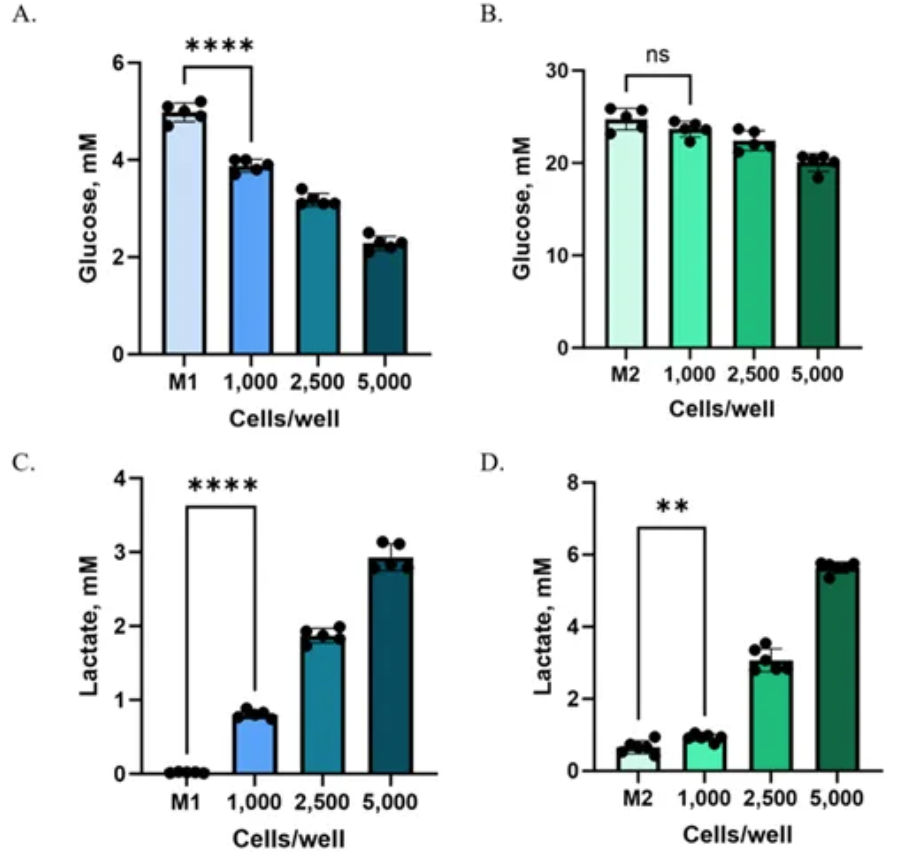
在较高细胞密度(每孔2,500和5,000个细胞)下,与对照相比,M1和M2培养基均显示出葡萄糖消耗和乳酸产生的明显变化(图3)。然而,在最低密度(每孔1,000个细胞)下,仅在M1中检测到变化。M1中较低的基线葡萄糖浓度和减少的背景代谢物创造了一个更灵敏的检测窗口,使得可以测量到在M2中被掩盖的细微变化。
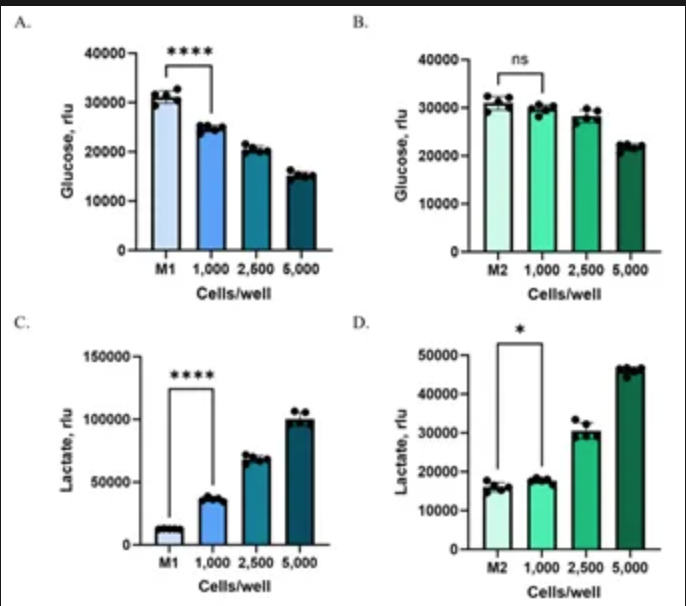
图3. HCT116球状体的葡萄糖消耗和乳酸分泌。将HCT116细胞以不同细胞密度(每孔1,000、2,500和5,000个细胞)接种于100μl M1培养基(含5 mM葡萄糖和5%透析血清的DMEM)或M2培养基(含25mM葡萄糖和10%胎牛血清的DMEM)中,使用康宁超低吸附96孔板。一组仅含培养基不含细胞的孔作为对照。细胞培养72小时以形成球状体,然后从每孔取出20μl培养上清液样品,与80μl PBS混合,随后冷冻保存样品。在运行代谢物检测当天,将样品解冻并用PBS进一步稀释(M1稀释至培养基原浓度的1:40,M2稀释至1:200)。接着,将9μl稀释后的样品转移至白色不透明低体积384孔板的选定孔中,并与9μl Glucose-Glo™ Assay(J6021)的检测试剂混合(A, B图),或与9μl Lactate-Glo™ Assay(J5021)的检测试剂混合(C, D图)。
将发光信号转换为绝对浓度后,凸显了不同的代谢物利用模式(图4)。在M2培养基中,葡萄糖仅小幅下降(高密度球状体中从25mM降至约20mM),且消耗速率在不同密度下保持稳定,约为每小时每细胞1.3-1.5nmol。相反,在M1培养基中,高密度下葡萄糖几乎耗尽(从5mM降至约2mM),消耗速率从低密度下的约每小时每细胞1.5nmol降至高密度下的约每小时每细胞0.75nmol。乳酸分泌遵循相同趋势:与M1相比(高密度下可低至每小时每细胞0.8nmol),M2中的分泌速率更高且更一致(约每小时每细胞1.3nmol)。这些结果表明,如M2中较高的代谢物浓度可以维持较大球状体中稳定的代谢活性。
图4. HCT116球状体中葡萄糖消耗(A, B)和乳酸分泌(C, D)的定量分析。葡萄糖和乳酸的标准曲线同步运行,以将发光信号转换为绝对浓度。数据代表五个生物学重复,误差线显示标准差。
该比较强调了培养基成分在影响检测结果方面的双重作用。如M1中较低的代谢物浓度,可增强检测细微代谢变化的灵敏度,尤其在较低的球状体密度下。相反,如M2中较高的代谢物浓度,则提供了维持较大球状体中细胞健康和一致代谢活性所需的营养供应。因此,在设计和解读3D模型中的代谢检测时,必须仔细考虑培养基成分和细胞密度。
案例研究2:利用代谢物检测法进行基于3D模型的抑制剂筛选
Promega的"加样-读数"生物发光代谢物检测法非常适用于自动化和高通量工作流程。其灵敏度允许小型化至384甚至1536孔板格式,使其成为在复杂3D模型中进行高通量代谢筛选的有效工具。为证明这一点,我们在一项使用球状体收集的培养基进行的聚焦抑制剂研究中应用了这些检测法。
我们选择了两种特征明确的代谢通路抑制剂用于HCT116球状体。使用糖酵解抑制剂2-脱氧-D-葡萄糖(2DG)(一种不可水解的葡萄糖类似物)来阻断乳酸生成,并通过384孔板形式的Lactate-Glo™ Assay进行测量。使用谷氨酰胺酶抑制剂BPTES(可阻止谷氨酰胺向谷氨酸的转化)来阻断谷氨酰胺分解,其变化通过同样以384孔板形式进行的Glutamate-Glo™ Assay测量。
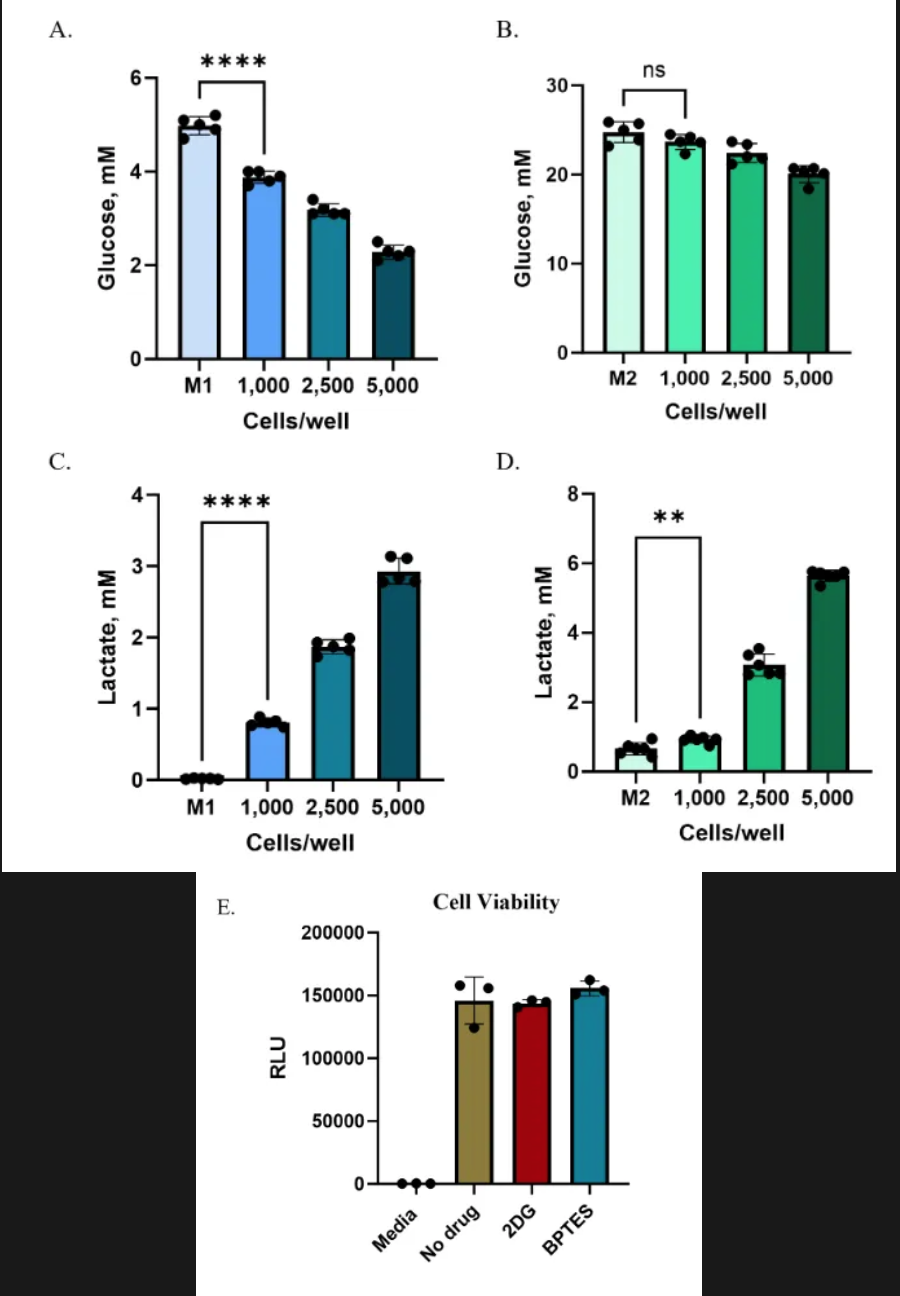
在处理开始时("0小时"),球状体孔中的乳酸和谷氨酸水平已经高于仅含培养基的对照,这反映了球状体形成期间的分泌以及采用了部分(50%)培养基更换策略。在24小时的处理期间,未经处理的球状体持续分泌代谢物:乳酸水平上升约200%(增加约1.4mM),谷氨酸上升约170%(增加约46µM)(图5A, B)。相比之下,2DG处理几乎完全消除了乳酸分泌(抑制率>90%),而BPTES使谷氨酸分泌减少了约65-70%(图5C, D)。
为确认代谢物水平的变化反映的是通路抑制而非细胞毒性,我们使用RealTime-Glo™ MT细胞活力检测系统测量了细胞活力。处理过的球状体的发光信号与未处理的对照组相当,表明2DG和BPTES在这些条件下没有毒性(图5E)。
这些结果表明,Promega的代谢物检测法可以有效地以小型化形式应用于3D球状体的抑制剂测试,能够可靠地检测通路特异性效应,同时保持与自动化和高通量工作流程的兼容性。
图5.
在3D模型中成功测量代谢物的关键要素总结
Promega的发光代谢物检测法为监测3D细胞模型中的代谢活性提供了一个灵敏且多功能的平台。这些检测法通过将代谢物特异性脱氢酶与NAD(P)H依赖性生物发光相结合,实现了更高灵敏度、宽线性范围和稳健的检测窗口。为在球状体和类器官研究中最大化其效用,研究人员应牢记以下因素:
优化培养基成分。选择生理相关的营养物水平(例如低葡萄糖)并使用透析血清,以尽量减少掩盖细微变化的背景代谢物。使培养条件与实验目标保持一致可提高灵敏度和生物学相关性。
考虑细胞密度效应。低密度球状体更易于检测细微变化,而较高密度可能需要营养丰富的培养基以维持稳定的代谢活性。进行多密度预实验有助于确定最佳条件。
采用部分培养基更换法进行操作。更换约50%的培养基可保持球状体完整性并减少孔间差异。尽管这会降低检测灵敏度,但提供了一个可重复且易于自动化的工作流程。
将代谢物检测与活力测量结合使用。平行地运行如RealTime-Glo™ MT细胞活力检测系统等可确保观察到的变化反映的是通路调节,而非细胞毒性。
利用可扩展性进行高效的高通量研究。"加样-读数"操作模式和发光检测信号使这些检测法高度兼容384和1536孔板格式,支持高效的抑制剂筛选及其他高通量应用。
参考文献
Peirsman, A., et al (2021). MISpheroID: a knowledgebase and transparency tool for minimum information in spheroid identity. Nature Methods, 18(11), 1294–1303. https://doi.org/10.1038/s41592-021-01291-4
资料下载