NLRP3炎性小体细胞水平药物发现综合工具箱
关键词:炎性小体,NLRP3抑制剂,高通量筛选,细胞水平定量检测,NanoBRET® TE,Caspase-1 激活和 IL-1β释放。
NLRP3炎性小体与多种疾病的发生密切相关,包括自身免疫性疾病和阿尔茨海默症。对这一蛋白质复合体的抑制将有望为炎症性疾病患者提供比当前广谱抗炎药物更为精准、针对性的缓解方案,且可能避免副作用。因此,评估NLRP3炎性小体作为治疗靶点的研究对于推进管线中潜在治疗药物至关重要。
以往,针对NLRP3炎性小体抑制剂的研究,主要依赖于使用纯化NLRP3蛋白的无细胞实验体系。然而,无细胞实验无法评估抑制剂在细胞微环境内与靶标的物理结合情况。它们无法揭示NLRP3抑制剂是否进入细胞、是否与靶标结合以及抑制剂结合的持续时间。因此,需要建立基于细胞的实验方法来探究细胞内NLRP3靶标与抑制剂之间的相互作用。

原文链接:https://doi.org/10.1016/j.chembiol.2023.09.016
近期发表在《Cell Chemical Biology》中的一篇文献中,描述了一个用于NLRP3激活的机制检测和定量的基于细胞水平的检测平台,该平台使用三种可扩展的基于细胞的方法:活细胞水平NLRP3抑制剂与靶点的结合检测,快速Caspase-1激活和IL-1β释放检测。这些检测方法一起提供了一个互补可高通量检测的平台,将NLRP3的结合与抑制功能性炎性小体响应联系起来。
炎症与炎性小体
炎症是多种疾病的驱动因素,环境中的有害物质,如构成空气污染的颗粒物,也会引发炎症。这类引发炎症的物质被称为病原相关分子模式(PAMPs)或损伤相关分子模式(DAMPs)。
DAMPs和PAMPs会导致炎症小体的蛋白质复合体的形成。这种复合体的形成会激活Caspase-1,进而导致IL-1β和IL-18的切割与激活,同时还会切割 Gasdermin D,使其在细胞膜上形成孔洞,进一步释放更多的炎症化合物。
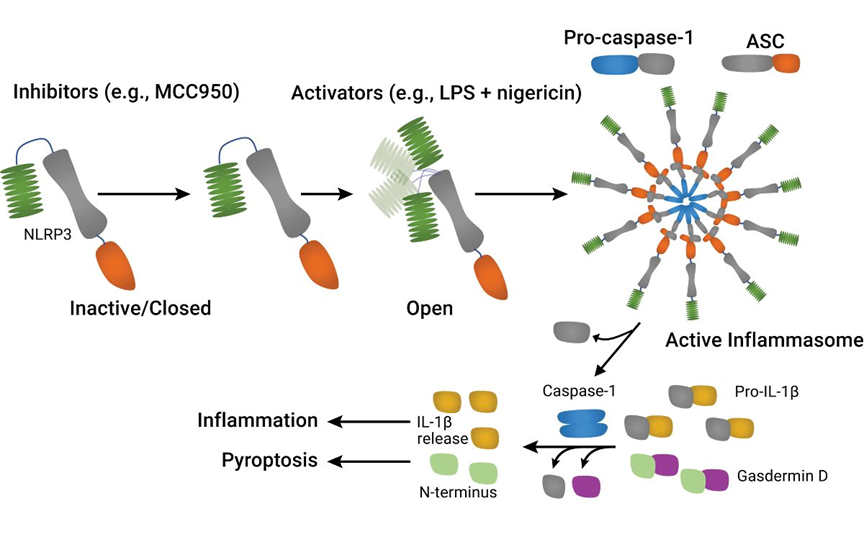
炎性小体的形成与慢性炎症和急性炎症疾病有关,也与环境因素引起的疾病有关。其中,对各种伤害均能作出响应的NLRP3炎症小体尤为引人关注。在PubMed上搜索“NLRP3 inflammasome”结果显示有超过 13,400 篇出版物。
检测NLRP3炎性小体激活的传统方法
1
显微镜检查
传统的免疫荧光染色技术使用特定的抗ASC抗体标记ASC斑点,以测量炎性小体的激活。虽然这种方法对于可视化ASC斑点蛋白的表达和定位很有用,但染色耗时长,需要多次洗涤步骤,而且不太适合高通量应用。
2
酶联免疫吸附测定(ELISA)
ELISA试剂盒用于量化炎性小体的激活,通常检测成熟形式的促炎细胞因子IL-1β和IL-18,或者分泌的HMGB1。但ELISA试剂盒仅检测蛋白质的存在,而不体现其激活状态,并且ELIASA耗时长,需要许多孵育和洗涤步骤,气线性范围也非常有限,样品通常需要稀释才能在适当范围内被检测到。
3
Western blot 和 Pull-down实验
Western blot被频繁用于评估通过加工促炎细胞因子(包括IL-1β和IL-18)以及Gasdermin D和其他各种caspases来实现的炎性小体激活。Western blot和Pull-down实验操作非常繁琐,需要针对感兴趣蛋白的特定一抗,是无法定量的。
更简便的监测炎性小体激活的方法
Promega提供了一系列可高通量且无需洗涤的简单的检测炎性小体激活的方法。
1
活细胞水平NLRP3抑制剂与靶点的结合检测
被广泛用于药物研发技术平台——NanoBRET® Target Engagement (TE) Assay。
NanoBRET® 是大幅改良的生物发光共振能量转移(BRET)分析平台,使用小而明亮的专利型NanoLuc® 萤光素酶作为能量供体和细胞可渗透的NanoBRET® TE tracer 作为能量受体。添加待测化合物后,化合物与 tracer 竞争靶蛋白的结合而导致BRET信号减弱。
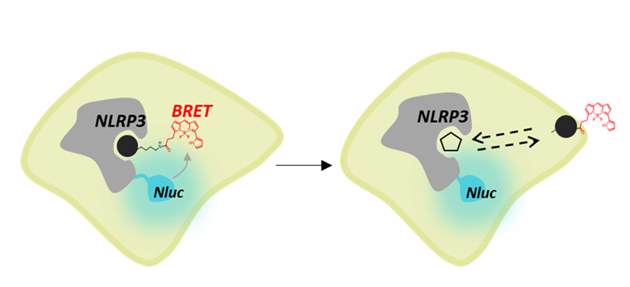
图1. NanoBRET® Target Engagement (TE) NLRP3 assay检测原理。在NLRP3检测中,将NanoLuc®- NLRP3融合表达载体转染到细胞中,然后加入相应的细胞穿透性荧光tracer。当荧光tracer与NanoLuc®- NLRP3融合蛋白结合时,会产生BRET信号。该tracer与目标的结合是可逆的,因此,如果存在其他与目标结合的分子(例如NLRP3抑制剂),竞争会导致示踪剂结合减少和BRET信号下降。
NanoBRET® TE Assay可以检测:
● 药物化合物进入细胞的能力(渗透性)
● 化合物与靶标分子结合的时间长短(滞留时间)
● 提供化合物对细胞内与靶标分子密切相关的蛋白质的结合数据(选择性)
● 量化化合物对靶标的结合强度和结合量(亲和力和占有率)。
2
Caspase-1激活检测
Caspase-Glo® 1 Inflammasome Assay 是一种结合酶系统的生物发光法检测试剂盒,使用Z-WEHD-氨基萤光素底物和Ultra-Glo™萤光素酶,用于监测Caspase-1活性。该方法仅测量具有催化活性的 Caspase-1 酶,无需样本制备,可快速完成检测。
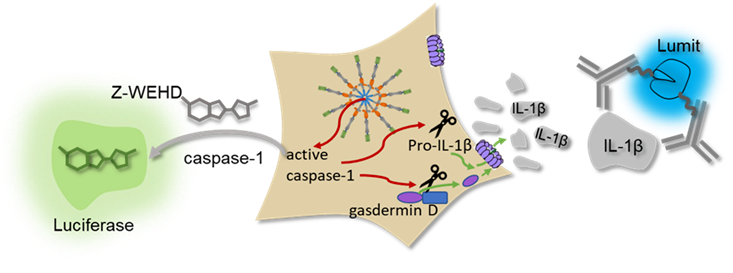
图2. 生物发光的基于细胞的测定方法检测分泌的IL-1β和caspase-1激活作为炎性小体激活的功能性读数。
3
IL-1β分泌检测
Lumit® IL-1β Human/Mouse Immunoassay采用NanoBiT®萤光素酶技术。抗体被分别标记上两种NanoBiT®亚基——小亚基(SmBiT)和大亚基(LgBiT)。当抗体与目标(IL-1β)结合时,SmBiT和LgBiT靠近从而产生生物发光信号。
Lumit® Cytokine Immunoassay 是均质法即用型检测试剂盒,简单的加样-读数操作模式无需洗涤,可以在70分钟之内快速简便的完成检测。同时可提供其他Lumit®即用型检测试剂盒,包含HMGB1, IL-18, IFN-γ, IL-2等十余种靶标。
4
使用炎性小体抑制剂MCC950对方法的验证
这三个炎性小体测定方法使用不同的技术来监测炎性小体激活途径中的不同机制。所有测定均可直接在细胞上进行,并且能够适应高通量需求。在三个测定中,MCC950的抑制显示出良好的IC50对应性,表明这些测定报告的是相同的NLRP3炎性小体途径,并为从靶点结合到细胞功能的炎性小体激活测量提供了一个坚实的平台(图3)。
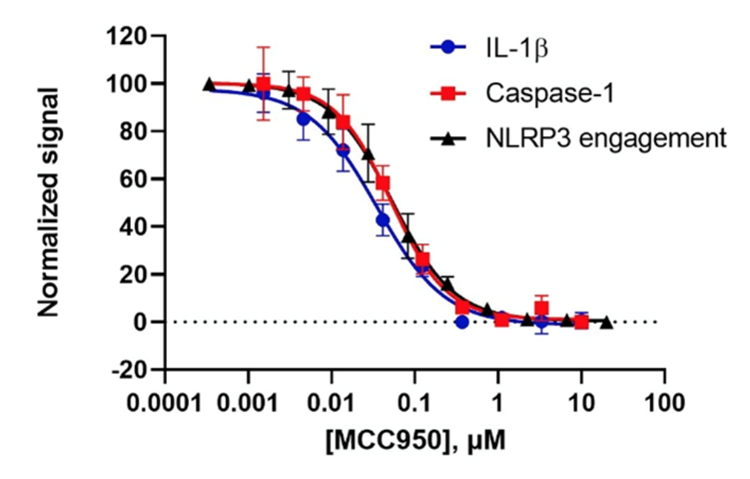
图3. 使用MCC950验证的三种炎性小体测定方法。
比较NLRP3炎性小体拮抗剂的效力
使用以上三种测定方法对NLRP3抑制剂,包括Oridonin、NBC19、NBC6和CY-09,进行效力排名。在所有三个测定中,MCC950是五种化合物中最有效的。它们的IC50值相差不大,功能测定中接下来最有效的化合物是Oridonin、NBC19和NBC6。在所有三个测定中,效力最低的化合物是CY-09。其结果得到了一致性验证。
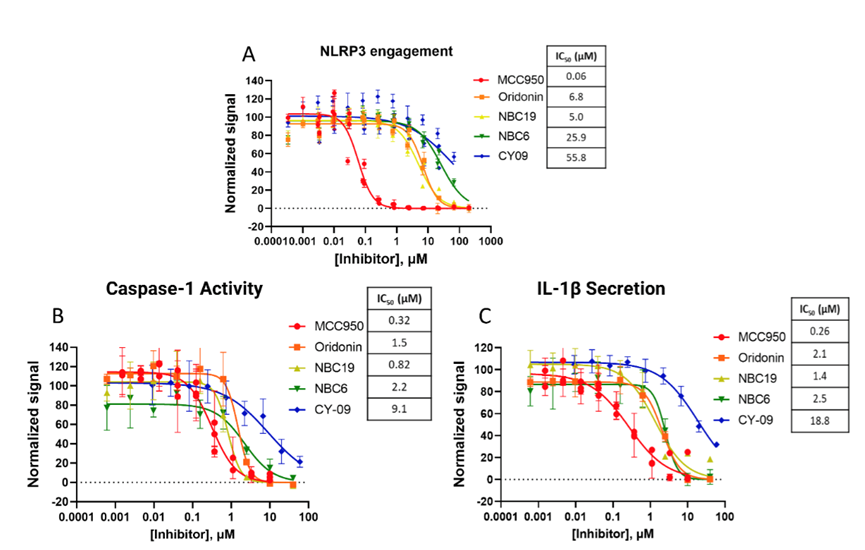
图4. NLRP3抑制剂的效力排名。A) HEK293细胞中NLRP3靶点接触。B) 用nigericin处理的LPS预处理PBMCs的Caspase-1活性。C) 用nigericin处理的LPS预处理PBMCs的IL-1β分泌。
炎性检测主要产品
|
应用 |
产品名称 |
目录号 |
|
Caspase-1活性 |
|
G9951 |
|
IL-1β分泌 |
|
W6010(Human) W7010(Mouse) |
|
NLRP3 NACHT 结构域亲和力检测 |
|
咨询Promega |
|
HMGB1检测 |
|
W6110 |
|
胞外ATP检测 |
|
GA5010 |
技术资源
炎性检测解决方案

炎性小体研究讲座

竞答有奖
前10名
可获得杜邦双肩包1个

问题
Promega可提供以下几种炎性小体细胞水平研究的方法:
1. Caspase-1活性检测 ;
2. 酶联免疫吸附测定(ELISA);
3. IL-1β分泌检测(快速且无洗涤);
4. 活细胞水平NLRP3 亲和力检测。
请在本次微信贴下方留言给出您的答案(回复序号即可,比如1)。回答正确的前10位小伙伴可获得时尚杜邦双肩包一个!
该活动解释权归普洛麦格(北京)生物技术有限公司所有。

产品信息

说明书查询

实验工具

技术资料









